Pneumotorax (PNO) je definovaný ako patologické nahromadenie vzduchu v pleurálnej dutine. V princípe ho môžeme kategorizovať ako traumatický a spontánny. Spontánny PNO potom môže byť ďalej klasifikovaný ako primárny, sekundárny a katameniálny. Podľa patofyziologickej povahy je PNO definovaný ako otvorený, uzavretý a tenzný.
Sú pre vás obrazové kazuistiky užitočné? Požadovali by ste obrazové kazuistiky aj z iných odborov? Máte nejaké pripomienky alebo návrhy na vylepšenie? Prosím, poskytnite nám váš názor vyplnením krátkeho dotazníka.
Incidencia spontánneho pneumotoraxu je 18-28/100 000 obyvateľov pre mužskú populáciu a 1,2-6/100 000 v populácii ženskej. V symptomatológii dominuje triáda symtómov: bolesť na hrudníku, dyspnoe a kašeľ. Zlatým štandardom v diagnostike ostáva RTG hrudníka v dvoch projekciách. Liečba je potom daná rozsahom PNO a klinickou symptomatológiou. Možnosti liečby sú dané od observácie a oxygenoterapie, cez ihlovú aspiráciu a trubicovú drenáž pleurálneho priestoru až po jednotlivé typy operačných intervencií. V dnešnej dobe sú preferované miniinvazívne techniky a to najmä videotorakoskopia (VTS) a video-asistovaná torakoskopia (VATS). Na diagnostiku, liečbu a optimálny manažment pacientov bolo recentne konštruovaných niekoľko svetovo akceptovaných odporúčaní. V našich geografických šírkach sa do popredia dostávajú najmä odporúčania formulované autormi z BTS (Britská torakálna spoločnosť − British Thoracic Society), ERS (Európska respiračná spoločnosť – European Respiratory Society) a ACCP (Americké kolégium hrudných špecialistov − American College of Chest Physicians).
Úvod:
Pneumotorax (PNO) znamená patologické nahromadenie vzduchu v pleurálnom priestore [1]. Termín pneumotorax bol prvýkrát definovaný kolektívom autorov pod vedením Itarda v roku 1803 a Laenneca v roku 1819 [2]. Ochorenie bolo definované ako kolekcia vzduchu v pleurálnom priestore, teda medzi pľúcami a hrudnou stenou. Tuberkulóza a jej komplikácie boli v týchto časoch opisované ako hlavná príčina vzniku. Pneumotorax sa však vyskytoval aj u niektorých zdravých pacientov bez tuberkulózy, či iných ochorení. V tých časoch bol takýto PNO označovaný ako pneumotorax simplex. Kjærgaard vo svojom diele používa prvýkrát pojem primárny spontánny pneumotorax (PSP) v roku 1932 [2].
Klasifikácia:
Pneumotorax môže byť klasifikovaný do dvoch veľkých skupín a to spontánny a získaný (obrázok 1). Získaný PNO je delený na iatrogény (napríklad ako komplikácia pľúcnej biopsie alebo komplikácia fibrobronchoskopie) a úrazový. Spontánny PNO je možné rozčleniť na primárny spontánny pneumotorax (PSP), sekundárny spontánny pneumotorax (SSP) a katameniálny pneumotorax [3]. Zatiaľ čo výskyt PSP je charakteristický u mladších vekových kategórií bez známeho pľúcneho ochorenia, výskyt SSP je vo väčšine prípadov asociovaný s chronickými pľúcnymi komorbiditami ako napríklad chronická obštrukčná choroba pľúc (CHOCHP). Katameniálny PNO predstavuje raritnú skupinu, kde je rozvoj PNO asociovaný s endometriózou. Endometrióza je definovaná ako výskyt endometriálnych žliazok mimo maternicovú dutinu [4] a jednou z manifestácií tohto ochorenia môže byť práve výskyt PNO.
Rizikové faktory a patofyziológia:
Rizikové faktory pre získaný PNO (úrazový a iatrogénny) sú dané povahou a charakterom úrazového mechanizmu a tiež povahou a charakterom zvolenej invazívnej/semiinvazívnej diagnostickej a terapeutickej modality. Práve preto musia byť pacienti pred realizáciou takýchto intervencií (CT navigovaná biopsia pľúc, bronchofibroskopia, pleurálne punkcie a iné) informovaní o možnostiach vzniku komplikácií a podpisujú pred podstúpením vyšetrenia informovaný súhlas s výkonom [3]. Hlavným rizikovým faktorom pre vznik PSP sa javí fajčenie tabakových výrobkov. Riziko vzniku stúpa s počtom vyfajčených cigariet za deň [5, 6].
Medzi ďalšie rizikové faktory sú zaraďované: nižšie hodnoty BMI, ↑ telesná výška, ↓ vek a pozitívna rodinná anamnéza [7]. Tiež stav znečistenia ovzdušia v jednotlivých regiónoch môže pôsobiť ako rizikový faktor vzniku PSP [3]. Pre SSP platí, že riziko vzniku je dané povahou základného ochorenia, teda najmä CHOCHP a cystickej fibrózy (CF). Vo všeobecnosti je možné konštatovať, že fajčenie tabakových výrobkov vo väčšom počte za deň a počas dlhšieho časového intervalu je hlavným rizikovým faktorom pre rozvoj PSP aj SSP [3]. Patofyziologická podstata rozvoja sekundárneho spontánneho PNO spočíva v ruptúre patologicky zmeneného pľúcneho tkaniva (spontánna ruptúra emfyzematóznych búl). Na druhej strane exaktný mechanizmus patogenézy PSP nie je doposiaľ objasnený. Väčšina autorov sa prikláňa k názoru, že PSP vzniká v dôsledku spontánnej ruptúry subpleurálných blebs a búl [8]. Prítomnosť týchto zmien je vizualizovateľná ipsi- aj bilaterálne pomocou CT vyšetrenia, či verifikovaná počas operácie. Tieto zmeny na viscerálnej pleure sú označované aj ako emfyzému podobné zmeny, z anglickej terminológie emphysema-like changes (ELCs) [6]. PSP potom vzniká ako dôsledok ruptúry ELCs a tento proces je známy ako Vanderschuerenova hypotéza. Zaujímavé je, že presná lokalizácia miesta ruptúry už počas operácie ani pri histologickom vyšetrení väčšinou nie je možná. V mikroskopickom obraze je väčšinou prítomný difúzny areál poškodených mezotelových buniek v oblasti viscerálnej pleury, ktorý je nahrádzaný vrstvou zápalových buniek. V týchto miestach dochádza k rozvoju fibroelastického procesu a formácii pórov o veľkosti 10 až 20 milimetrov. Výsledkom je vznik difúzneho pleurálneho porózneho areálu [6, 9]. Táto skutočnosť bola verifikovaná štúdiami využívajúcimi metódy autoflorescenčnej torakoskopie [10].
Symptomatológia a diagnostika:
Symptomatológia a diagnostika: Bez ohľadu na etiológiu je základná triáda symptómov asociovaných s rozvojom PNO daná nasledovne: bolesť na hrudníku, dyspnoe a kašeľ. Samotná klinická manifestácia je však podmieňovaná viacerými faktormi. Jedným z najdôležitejších takýchto faktorov je rozsah pneumotoraxu. Ten sa môže pohybovať v rozmedzí od pláštového PNO, PNO malých rozmerov až po úplný kolaps pľúcneho krídla v príslušnom hemitoraxe. Na posúdenie veľkosti PNO je nevyhnutné použitie zobrazovacej techniky a to v podobe RTG alebo CT vyšetrenia. Limitácia natívnej RTG snímky v PA projekcii spočíva v dvojdimenzionálnom zobrazení, kým pleurálna dutina je trojdimenzionálna anatomická štruktúra. Dôležité je pochopenie, že prítomnosť 2 cm PNO pri RTG PA vyšetrení môže znamenať redukciu pľúcneho objemu na postihnutej strane až o 50 % [7]. Na určenie veľkosti PNO je tiež v niektorých štúdiách definovaný Lightov index [6]. Využitie CT vyšetrenia a následné meranie vzdialenosti medzi hrudnou stenou a povrchom pľúc v úrovni pľúcneho hilu alebo meranie vzdialenosti od apexu pľúc ku kupole (v PACS) sa javí ako najpresnejšia modalita na posúdenie veľkosti pneumotoraxu (obrázok 2) [7]. Veľkosť PNO však nie vždy koreluje s klinickou manifestáciou ochorenia. Táto skutočnosť je zvýraznená najmä pri rozvoji SSP. U týchto pacientov ( CHOPCH, CF) vedie aj prítomnosť RTG PNO malých rozmerov k signifikantnému klinickéu zhoršeniu a preto sa na túto skutočnosť musí prihliadať aj pri voľbe liečebnej modality. Diagnostika PNO je daná kombináciou adekvátnej odobratých anamnestických údajov, zodpovedne realizovaného fyzikálneho vyšetrenia (vrátane auskultácie) a vhodne zvolenej zobrazovacej techniky. Zlatým štandardom diagnostiky PNO ostáva RTG vyšetrenie hrudníka v dvoch projekciách (obrázok 3) [3, 6, 7]. Využitie počítačovej tomografie (CT) vykazuje vyššiu senzitivitu v diagnostike PNO. Pomocou CT vyšetrenia je možné presne určiť rozsah/veľkosť ochorenia a za použitia tejto diagnostickej modality sú detegovateľné aj pomerne malé pneumotoraxy (obrázok 4) [11]. Komplexnejší a detailnejší obraz pri CT vyšetrení hrudníka je tiež nápomocný pri diagnostike bulózneho emfyzému a iných pľúcnych komorbidít bilaterálne. Nevýhody počítačovej tomografie predstavujú vyššiu radiačnú záťaž najmä u mladých pacientov/tok s PSP a tiež vyššie finančné náklady v porovnaní s RTG projekciami. Práve z tohto hľadiska nie je CT vyšetrenie indikované ako iniciálna zobrazovacia modalita [6,7]. Ďalšia alternatívna diagnostická možnosť je prezentovaná ultrasonografickým (USG) vyšetrením. USG hrudníka predstavuje pomerne senzitívnu metódu v detekcii PNO. Vo všeobecnosti však rutinné využitie USG pri diagnostike PSP nie je zaužívané [3].
Liečba:
Pneumotorax je náhla príhoda, ktorá môže pacienta ohroziť nie len na zdraví ale aj na živote. Ako je to spomenuté vyššie liečba závisí od etiológie, veľkosti PNO a najmä klinického stavu pacienta. Observácia a oxygenoterapia je možná len u plášťových PNO a u pacientov bez prítomnosti rizikových faktorov. Vo väčšine prípadov je indikovaná ihlová aspirácia alebo trubicová drenáž. Drenáž pleurálneho priestoru je život zachraňujúca urgentná procedúra. Využívané sú hrudné drény rôznych rozmerov. Vo väčšine prípadov je táto intervencia realizovaná v lokálnej anestéze (mezokaín). Na torakochirurgických pracoviskách zavádzame hrudné drény v úrovni štvrtého medzirebria a to v strednej axilárnej čiare. Koniec drénu je potom v prípade PNO smerovaný apikálne. Hrudný drén je fixovaný ku koži pomocou stehov. Drén je napojený na sofistikované systémy aktívneho odsávania a neskôr ponechaný na pasívnej drenáži. Pokiaľ dôjde k opätovnému rozvinutiu pľúcneho tkaniva a nie je pozorovaný pretrvávajúci airleak je možná extrakcia hrudného drénu. Indikácie k operačnej intervencii v celkovej narkóze sú nasledovné:
- prítomnosť bilaterálneho PNO,
- sekundárny atak PNO na ipsilaterálnej strane,
- prvý atak PNO na kontralaterálnej strane,
- perzistujúci airleak alebo nemožnosť dosiahnutia úplnej reexpanzie pľúcneho parenchýmu,
- pneumohemotorax,
- pacienti s rizikovými povolaniami (piloti, potápači).
Samotná operačná intervencia je potom realizovaná na pracovisku torakálnej chirurgie a to otvorenou cestou (torakotómia) alebo miniinvazívne (VTS, VATS). Podstatou operácie je ošetrenie chorobne zmeneného tkaniva pľúc (buly) a to pomocou atypickej resekcie za použitia staplerov (resekcia pľúcneho hrotu, volum redukčné operácie) alebo v niektorých prípadoch až v rozsahu lobektómie. Na zabráneniu recidívy ochorenia je využívaná metodika mechanickej pleurodézy v podobe parciálnej pleurektómie a pleurabrázie [3].
Kazuistika
Anamnéza:
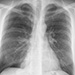
V priloženej kazuistike je demonštrovaný prípad mladého 27 ročného pacienta, ktorý bol prijatý na kliniku hrudnej chirurgie po ošetrení na internej ambulancii urgentného príjmu pre bolesti na hrudníku a dyspnoe. V rámci diferenciálnej diagnostiky bola indikovaná realizácia RTG hrudníka, kde bola potvrdená prítomnosť pneumotoraxu na pravej strane (obrázok 5). Internista vylúčil kardiálnu príčinu ťažkostí a pacient bol odovzdaný k ďalšiemu manažmentu do rúk hrudného chirurga.
Z anamnestických údajov sa jednalo o doteraz zdravého jedinca, u ktorého neboli prítomné žiadne komorbidity. Pacient neužíval dlhodobo žiadnu medikamentóznu terapiu a tiež u neho nebola zistená prítomnosť alergií. Jednalo sa o nefajčiara aj keď bolo zistené, že v minulosti krátkodobo pracoval ako barman a pohyboval sa aj v priestoroch s expozíciou tabakového dymu. Konzumáciu alkoholu udával len striedmo – príležitostne. Aktuálne prišiel na ošetrenie lebo ho asi dva dni dozadu pri práci (dvíhal ťažšie predmety) začalo pichať na hrudníku. Pri vyšetrení na torakochirurgickej ambulancii priznával, že posledný deň sa mu už aj ťažšie dýcha a preto vyhľadal lekársku pomoc.
Vyšetrenie:
Fyzikálne vyšetrenie odhalilo vymiznuté dýchanie v úrovni pravého hemitoraxu. Vzhľadom na anamnézu, fyzikálny nález a RTG dokumentáciu bol indikovaný urgentný príjem na II. chirurgickú kliniku UPJŠ–LF a UNLP v Košiciach. Pacient bol prijatý na jednotku intenzívnej starostlivosti (JIS), kde bol okamžite realizovaný kontinuálny monitoring vitálnych funkcií. Nakoľko bol pacient hemodynamicky stabilný a saturácie pri oxygenoterapii boli 96% bolo možné realizovať nevyhnutné predoperačné vyšetrenia. U pacienta boli realizované odbery krvi na hematologické, hemokoagulačné a biochemické vyšetrenia. Tiež bola vyšetrená krvná skupina pacienta. Výsledky vyšetrení boli vo fyziologickom rozhraní.
Terapia:
Vzhľadom na prítomnosť symptomatického PNO väčších rozmerov bola indikovaná urgentná drenáž pleurálneho priestoru. Samotná procedúra bola realizovaná v priestoroch operačného traktu II. cirurgickej kliniky UPJŠ-LF a UNLP v Košiciach a to v lokálnej anestéze (mezokaín). Chirurg si pred realizáciou intervencie skontroloval výsledky laboratórnych vyšetrení (najmä hemokoagulačné vyšetrenie) a opätovne si overil alergologickú a liekovú anamnézu pacienta. Pred samotnou drenážou bola opätovne prezretá obrazová dokumentácia (RTG hrudníka) a potvrdená stranová verifikácia. Hrudný drén bol zavedený v piatom medzirebrovom priestore v úrovni prednej axilárnej čiary vpravo a fixovaný pomocou kožných stehov. Pacient bol transportovaný na JIS a drén napojený na systém aktívneho odsávania. Pacient toleroval intervenciu dobre a kontrolná RTG hrudníka potvrdzuje správnu polohu drénu intrapleurálne. Tiež je prítomné už úplné rozvinutie pľúcneho tkaniva (obrázok 6). V liečbe je podávaný nizkomolekulárny heparín (LMWH) v profylaktickej dávke, ATB krytie, mukolytiká a analgetiká. Hrudný drén ostáva na aktívnom odsávacom systéme po dobu 48 hodín. Následne je drén napojený na pasívnu drenáž. Airleak, ktorý by znamenal prítomnosť perzistujúceho PNO nebol pozorovaný. Pacient bol preložený na štandardné oddelenie. Nasledujúci deň bol hrudný drén uzavretý (peanovaný) a bola realizovaná kontrolná RTG hrudníka s odstupom 12 hodín (obrázok 7). Na snímke je prítomné úplné rozvinutie pľúcneho tkaniva a PNO nie je prítomný. Vzhľadom na uvedené je možné konštatovať, že liečba bola úspešná a hrudný drén preto mohol byť následne extrahovaný. Pacient je observovaný na klinike hrudnej chirurgie ešte nasledujúci deň a následne prepustený domov.
Diskusia:
Zhrnutie tejto kazuistiky môže byť prezentované nasledovne. U mladého pacienta bez akýchkoľvek komorbidít bola prítomá bolesť na hrudi a progredujúce dyspnoe, čo viedlo k suspekcii na diagnózu primárneho spontánneho PNO. Táto diagnóza bola nakoniec potvrdená RTG vyšetrením a pacient bol urgentne torakochirurgicky manažovaný a to cestou hrudnej drenáže. Samotná operačná intervencia ako aj pooperačný priebeh boli bez závažných komplikácií. U pacienta nebol pozorovaný perzistujúci airleak a kontrolné RTG hrudníka boli vyhovujúce. Preto bola možná extrakcia hrudného drénu a postupné ukončenie hospitalizácie. Pacient bol prepustený v dobrom stave domov. Dôležité je si uvedomiť, že pacient ostáva v pneumologickom dispenzári a je tiež poučený o možnosti recidívy ochorenia na ipsi aj kontralaterálnej strane.
Literatúra:
[1] Kováč I, Varga P, Kudláč M, et al. Pľúcna forma lymfangioleiomyomatózy komplikovaná výskytom pneumotoraxu u mladého pacienta – kazuistika. Slov. chir. 2016;13(3- 4):83-84.
[2] Kjærgaard H. Spontaneous pneumothorax in the apparently healthy. Acta Med. Scand. (Suppl) 1932;43:1e159.
[3] Kováč I, Mikločová M, Stebnický M, et al. Diagnostika, liečba a odporúčania pre manažment primárneho spontánneho pneumotoraxu. Slov. chir. 2021;18(3):90-94.
[4] Kováč I, Novotný M, Kováčová K, et al. Endometrióza v jazve po cisárskom reze: naše recentné skúsenosti. Rozhl. Chir. 2021;100:27-31. doi: 10.33699/PIS.2021.100.1.27–31.
[5] Kim D, Eom SY, Shin CS, et al. The clinical effect of smoking and environmental factors in spontaneous pneumothorax: a case-crossover study in an Inland province. Ther. Adv. Respir. Dis. 2020;14:1753466620977408. doi: 10.1177/1753466620977408. PMID: 33287644; PMCID: PMC7727044.
[6] Tschopp JM, Bintcliffe O, Astoul P, et al. ERS task force statement: diagnosis and treatment of primary spontaneous pneumothorax. Eur. Respir. J. 2015;46(2):321-35. doi: 10.1183/09031936.00219214. Epub 2015 Jun 25. PMID: 26113675.
[7] Macduff A, Arnold A, Harvey J. BTS Pleural Disease Guideline Group. Management of spontaneous pneumothorax: British Thoracic Society Pleural Disease Guideline 2010. Thorax. 2010;65 Suppl 2:ii18-31. doi: 10.1136/thx.2010.136986. PMID: 20696690.
[8] Noppen M. Spontaneous pneumothorax: epidemiology, pathophysiology and cause. Eur. Respir. Rev. 2010;19(117):217- 9. doi: 10.1183/09059180.00005310. PMID: 20956196.
[9] Radomsky J, Becker HP, Hartel W. Pleural porosity in idiopathic spontaneous pneumothorax. Pneumologie. 1989;43(5):250-3. PMID: 2740304.
[10] Noppen M, Dekeukeleire T, Hanon S, et al. Fluorescein-enhanced autofluorescence thoracoscopy in patients with primary spontaneous pneumothorax and normal subjects. Am. J. Respir. Crit. Care. Med. 2006;174(1):26-30. doi: 10.1164/ rccm.200602-259OC. Epub 2006 Apr 20. PMID: 16627865.
[11] Almajid FM, Aljehani YM, Alabkary S, et al. The accuracy of computed tomography in detecting surgically resectable blebs or bullae in primary spontaneous pneumothorax. Radiol. Med. 2019;124(9):833-837. doi: 10.1007/s11547-019-01044-6. Epub 2019 May 27. PMID: 31134432.
Autori deklarujú, že kazuistiku s identickým obsahom nebudú publikovať v iných domácich alebo zahraničných printových alebo elektronických publikáciách.
Klasifikácia ICD-10:
Predmety/kurzy
Súvisiace články:
 Obsah článku podlieha licencii Creative Commons Uveďte autora-Neužívejte dílo komerčně-Nezasahujte do díla 3.0 Česko
Obsah článku podlieha licencii Creative Commons Uveďte autora-Neužívejte dílo komerčně-Nezasahujte do díla 3.0 Česko
citácia: Ivan Kováč: Pneumotorax: Manažment pacientov a kazuistika z nášho pracoviska. Multimediálna podpora výučby klinických a zdravotníckych odborov :: Portál Lekárskej fakulty Univerzity Pavla Jozefa Šafárika v Košiciach [online] , [cit. 17. 05. 2026]. Dostupný z WWW: https://portal.lf.upjs.sk/clanky.php?aid=491. ISSN 1337-7000.